Những biến thể COVID-19 nào có ở Việt Nam?
Việt Nam đang có những biến thể nào? Biến thể Ấn Độ nguy hiểm như thế nào? TTND.GS.TS Nguyễn Văn Kính, Chủ tịch Hội Truyền nhiễm Việt Nam sẽ trả lời quý bạn đọc trong chương trình giao lưu trực tuyến ngày 10/5/2021. Kết quả giải trình tự gene virus của Viện Vệ sinh dịch tễ Trung ...
HYH - E10 - Poster Link đăng ký tham dự TẠI ĐÂY:https://dang-ky.ecademy.vn/hyh-e10
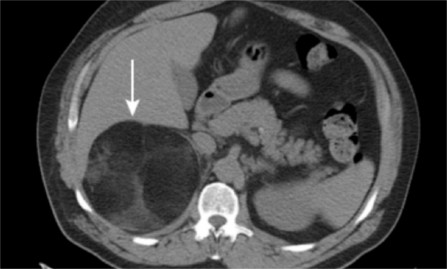
Cập nhật xử trí u thượng thận tình cờ
TS.BS Trần Quang Nam BM nội tiết ĐHYD Khoa nội tiết BV Nhân dân 115 tải về
B.S. Trần Ngọc Bảo Viêm tuỵ cấp (VTC) là một bệnh thường được gặp ở khoa cấp cứu các bệnh viện với bệnh cảnh cơn đau bụng cấp. Ở Mỹ mỗi năm có khoảng 220.000 bệnh nhân VTC được điều trị và số bệnh nhân VTC đã tăng gấp đôi trong 2 thập niên cuối. Ở Hà Lan từ 1992 ...